1. Comprendre la notion de verrou mécanique
Le trajet du nerf pudendal impose le franchissement de passages anatomiquement étroits. En conditions physiologiques, ces zones n’induisent pas de douleur. Elles deviennent des verrous mécaniques lorsque leur géométrie est défavorablement modifiée (posture, contraintes répétées) ou lorsque les tissus environnants perdent leur capacité d’adaptation (Robert et al., 1998).
Un verrou mécanique n’est pas forcément une lésion. Il peut correspondre à une zone où le nerf est agressé par compression intermittente, friction ou cisaillement répété. Cela explique un tableau clinique souvent fluctuant : exacerbations en assise, accalmies en décharge, variations selon les activités et la durée d’exposition aux contraintes (Labat et al., 2008/2023).
Dans la névralgie pudendale, le symptôme n’indique pas toujours « une lésion », mais peut révéler un contexte mécanique défavorable où le nerf est sur-sollicité au-delà de sa capacité d’adaptation (Labat et al., 2008/2023).
2. La pince ligamentaire : le conflit pivot
Le nerf pudendal traverse une zone critique au niveau de l’épine ischiatique, à proximité des ligaments sacro-épineux et sacro-tubéral. Cette région constitue la pince ligamentaire, décrite comme un mécanisme anatomique majeur d’irritation du nerf (Robert et al., 1998).
La particularité de ce conflit est sa forte dépendance à la posture. Lors de la station assise prolongée — notamment en rétroversion pelvienne (bassin « basculé en arrière ») — la tension ligamentaire peut augmenter, réduisant l’espace disponible pour le nerf et augmentant les contraintes de compression/cisaillement (Labat et al., 2008/2023).

Ce modèle explique une caractéristique classique : l’aggravation en assise. Il n’implique pas que l’assise soit « la cause unique », mais qu’elle peut être un facteur de contrainte qui révèle ou entretient un conflit préexistant (Labat et al., 2008/2023).
3. Le canal d’Alcock : un tunnel anatomique contraint
Après la région de l’épine ischiatique, le nerf pudendal chemine dans le canal d’Alcock (Alcock’s canal), un tunnel fascial formé par un dédoublement du fascia du muscle obturateur interne (Robert et al., 1998).
Dans cette page, le canal d’Alcock est abordé comme un verrou anatomique : un espace limité où le nerf et les vaisseaux associés peuvent subir une augmentation de contraintes mécaniques lorsque le volume du tunnel est réduit ou lorsque les tissus environnants sont hypertoniques (Cholewa et al., 2024).
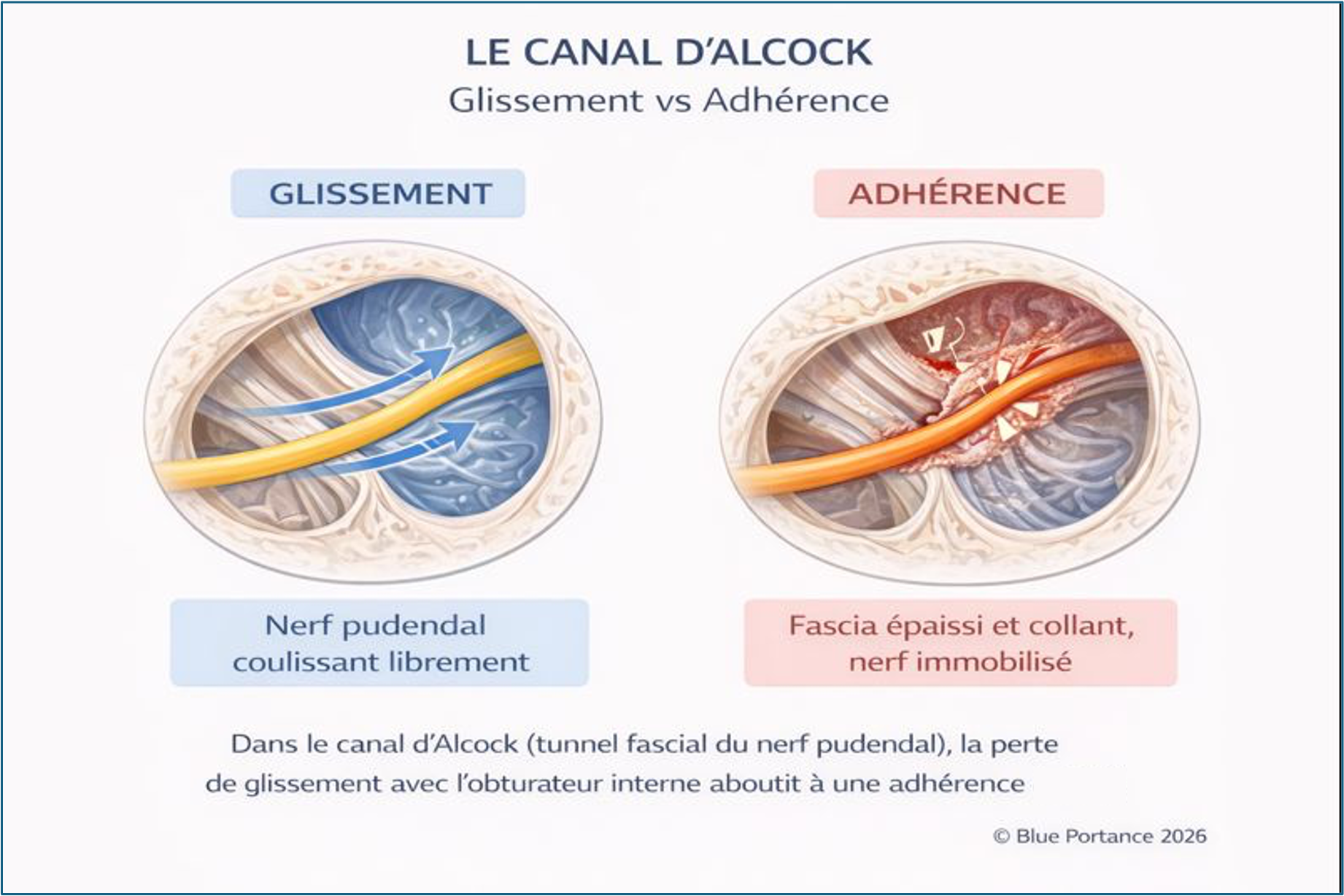
Un point essentiel pour la lecture BDC : une souffrance du nerf dans le canal d’Alcock peut relever d’un mécanisme strictement « géométrique » (verrou), ou d’un mécanisme plus subtil de perte de mobilité tissulaire. La distinction fait partie des pages de triage et de fascias (Stecco & Stecco, 2024).
4. Cumul des verrous et variabilité des symptômes
Les verrous mécaniques n’agissent que rarement de manière isolée. Un conflit modéré au niveau de la pince ligamentaire peut devenir symptomatique s’il se combine à une contrainte dans le canal d’Alcock, ou s’il s’associe à une hypertonie musculaire de protection (Cholewa et al., 2024).
Ce cumul explique la variabilité des tableaux : douleur fluctuante, alternance de périodes calmes et d’exacerbations, sensibilité particulière à l’assise prolongée, et réponses différentes selon les postures et les contextes (Labat et al., 2008/2023).
Références scientifiques
- Robert, R., Prat-Pradal, D., Labat, J.-J., et al. (1998). Anatomical basis of pudendal nerve entrapment. Surgical and Radiologic Anatomy. (Base anatomique des zones de conflit : pince ligamentaire, canal d’Alcock.)
- Labat, J.-J., Riant, T., Robert, R., et al. (2008; mise à jour 2023). Diagnostic criteria for pudendal neuralgia by pudendal nerve entrapment (Nantes criteria). (Références cliniques sur les caractéristiques de la douleur et la dépendance posturale.)
- Cholewa, J., et al. (2024). Myofascial entrapment in the Alcock’s canal: The role of pelvic floor hypertonia. (Lien entre hypertonie pelvienne et contraintes dans le canal d’Alcock.)
- Stecco, A., & Stecco, C. (2024). Fascial densification and neuropathic pain: clinical implications. (Modèle de densification et perte de mobilité tissulaire.)


