1. Le fascia comme milieu mécanique fonctionnel
Le système fascial pelvien constitue un continuum tissulaire organisant la relation mécanique entre structures nerveuses, musculaires et osseuses. Il ne s’agit pas d’un simple tissu d’enveloppe, mais d’un milieu mécanique actif, dont les propriétés conditionnent la manière dont les contraintes sont transmises, amorties ou dissipées lors du mouvement et des variations posturales (Stecco & Stecco, 2024).
D’un point de vue clinique-fonctionnel, la qualité du fascia ne se juge pas à son apparence morphologique, mais à sa capacité à autoriser des mobilités relatives fines entre les structures qu’il relie. Cette mobilité relative constitue une condition indispensable à la tolérance mécanique du nerf pudendal lors des mouvements du bassin, de la hanche et de la posture assise.
L’interface nerf-fascia, et en particulier la relation entre l’épinèvre du nerf pudendal et le fascia de l’obturateur interne, représente ainsi un déterminant fonctionnel majeur. Toute altération de cette interface modifie le régime mécanique auquel le nerf est soumis, indépendamment de l’existence d’une compression franche ou d’une lésion visible.
2. Neurodynamique : le glissement comme impératif clinique
Le glissement neural correspond à la capacité d’un nerf à se déplacer relativement aux tissus environnants lors des mouvements. Sur le plan clinique, ce phénomène constitue une exigence mécanique fondamentale : le système nerveux forme une structure continue, contrainte de s’adapter en permanence aux variations de longueur et de trajectoire induites par le mouvement (Butler, 2000).
Lorsque le glissement est préservé, les contraintes mécaniques sont redistribuées de manière diffuse et restent compatibles avec la physiologie nerveuse. Le nerf dispose alors d’une véritable réserve de mobilité, lui permettant de tolérer des changements posturaux importants sans déclencher de signal douloureux.
À l’inverse, la perte de mobilité relative transforme des sollicitations ordinaires — s’asseoir, se redresser, marcher — en sources d’agression mécanique répétée. Le nerf devient mécaniquement vulnérable : chaque mouvement induit une augmentation locale des contraintes de traction et de cisaillement, abaissant progressivement le seuil de tolérance neuropathique.
3. Densification fasciale et perte de tolérance mécanique
Dans la névralgie pudendale, l’analyse strictement localisée de la douleur se heurte rapidement à ses limites. L’opposition classique entre douleur dite « locale » et douleur qualifiée « d’irradiée » ne permet pas de rendre compte de tableaux cliniques où la symptomatologie fluctue selon la posture, la durée d’exposition à la position assise et la répétition des contraintes, sans continuité lésionnelle identifiable (Labat et al., 2008 ; Robert et al., 1998).
Une lecture fonctionnelle fondée sur la continuité tissulaire permet de dépasser cette opposition artificielle. Dans le réseau fascial pelvien, les contraintes mécaniques ne se transmettent pas de manière ponctuelle, mais selon une logique distribuée : une altération locale de la dynamique tissulaire peut modifier le régime mécanique global auquel sont soumises les structures adjacentes, sans qu’il existe pour autant de projection nerveuse directe ou de compression anatomique isolée (Stecco & Stecco, 2024).
La densification fasciale correspond à ce type d’altération fonctionnelle. Elle désigne une modification progressive des propriétés mécaniques du fascia, caractérisée par une diminution de la capacité de glissement entre les plans tissulaires. Il ne s’agit pas d’une lésion, mais d’une adaptation à un environnement mécanique appauvri en variations, tel qu’observé dans les situations de contraintes posturales maintenues, en particulier lors de la position assise prolongée (Stecco & Stecco, 2024).
À l’échelle clinique-fonctionnelle, le fascia peut être envisagé comme un matériau hydrophile dont les propriétés mécaniques dépendent de sa capacité à se réorganiser sous contrainte. Lorsque cette capacité est préservée, les plans tissulaires conservent une faible friction relative et autorisent les micro-déformations nécessaires à l’adaptation au mouvement. Lorsque cette dynamique se réduit, le tissu perd sa fluidité fonctionnelle et se comporte comme un milieu à déformation réversible limitée, augmentant les forces de cisaillement au sein des interfaces tissulaires (Stecco & Stecco, 2024).
© Blue Portance — 2026
Cette transformation du régime mécanique fascial ne reste pas confinée au tissu lui-même. En réduisant la mobilité relative entre les structures, elle modifie l’environnement mécanique des éléments qui dépendent de ce glissement pour tolérer les contraintes du mouvement. Le système fascial, organisé en réseau continu, transmet alors ces contraintes de manière distribuée, pouvant affecter des zones anatomiquement distinctes sans atteinte nerveuse périphérique directe (Stecco & Stecco, 2024).
Le nerf pudendal, intimement couplé à ces interfaces fasciales tout au long de son trajet pelvien, se trouve particulièrement exposé à ces modifications. Lorsque la densification s’installe, le nerf n’est plus libre de ses micro-déplacements. Il n’est pas comprimé de façon statique, mais soumis à des micro-agressions répétées à chaque variation posturale, en particulier lors du passage à la position assise ou du maintien prolongé de celle-ci (Cholewa et al., 2024).
Cette situation suffit à expliquer l’émergence et la persistance d’une douleur neuropathique en l’absence de toute lésion anatomique objectivable. La douleur ne résulte pas d’un « pincement » isolé, mais d’une perte de compatibilité mécanique entre le nerf et son environnement tissulaire, abaissant progressivement le seuil de tolérance aux contraintes ordinaires et favorisant la chronicisation des symptômes (Cholewa et al., 2024 ; Stecco & Stecco, 2024).
4. Le canal d’Alcock : dispositif de guidage dynamique et zone de vulnérabilité fonctionnelle
Le canal d’Alcock occupe une place centrale dans la compréhension de la névralgie pudendale, précisément parce qu’il concentre plusieurs facteurs de vulnérabilité mécanique sans constituer, en lui-même, une zone de compression pathologique systématique (Robert et al., 1998 ; Labat et al., 2008). Une lecture strictement anatomique, assimilant le canal à un simple « tunnel » rigide susceptible de pincer le nerf, s’avère insuffisante pour expliquer la majorité des tableaux cliniques observés.
Sur le plan fonctionnel, le canal d’Alcock correspond à un dédoublement du fascia de l’obturateur interne, formant un dispositif de guidage destiné à accompagner le nerf pudendal dans une région soumise à d’importantes variations mécaniques (Robert et al., 1998). Il ne s’agit pas d’un espace passif, mais d’une interface dynamique, conçue pour permettre au nerf de suivre les mouvements du bassin et de la hanche tout en limitant les contraintes excessives.
Cette fonction de guidage repose sur une condition essentielle : la capacité de glissement du nerf au sein de son environnement fascial. Tant que cette mobilité relative est préservée, le canal joue un rôle protecteur, permettant au nerf de s’adapter aux changements de posture et aux mouvements pelviens sans accumulation de contraintes mécaniques locales (Butler, 2000).
Lorsque la dynamique fasciale est altérée — par densification, hypertonie des muscles adjacents ou contraintes posturales répétées — le fonctionnement du canal se modifie profondément (Stecco & Stecco, 2024 ; Cholewa et al., 2024). Le dispositif de guidage perd sa capacité d’adaptation et devient une zone de friction mécanique accrue. Le nerf n’est pas comprimé de façon statique, mais exposé à des micro-agressions répétées à chaque variation posturale.
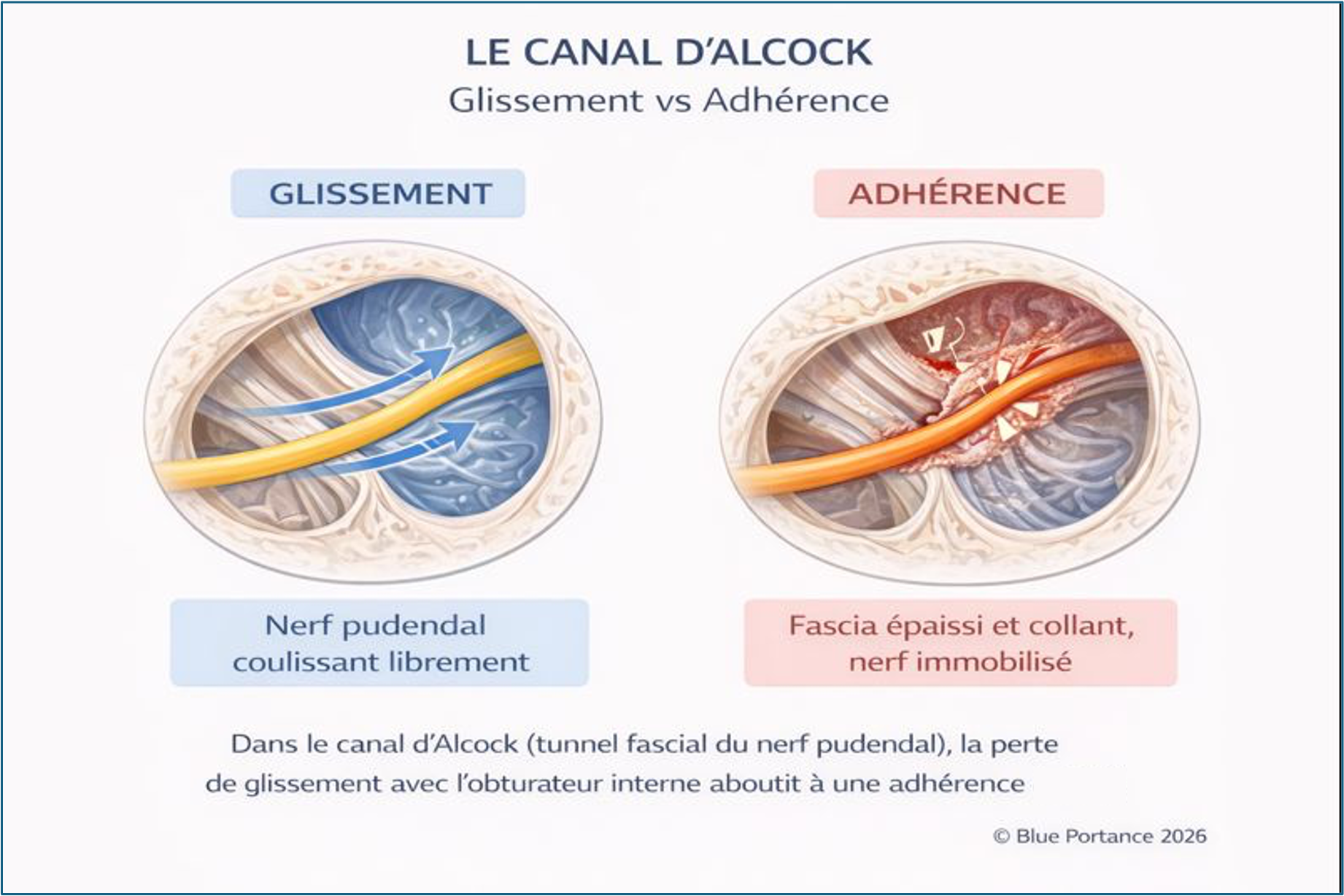
Cette lecture fonctionnelle permet de comprendre pourquoi le canal d’Alcock est fréquemment impliqué dans la symptomatologie sans qu’aucune sténose franche ne soit objectivable à l’imagerie (Labat et al., 2008). La douleur ne résulte pas d’un conflit structurel isolé, mais d’un défaut d’adaptation mécanique dans une zone où le nerf est particulièrement dépendant de la qualité des interfaces tissulaires.
Sur le plan clinique, cette vulnérabilité se manifeste par une douleur fortement dépendante de la posture et de la durée d’exposition. La position assise prolongée, en réduisant les micro-variations de mouvement et en augmentant les contraintes locales, accentue les phénomènes de friction et d’irritation dans le canal (Cholewa et al., 2024). À l’inverse, les variations posturales ou les phases de décharge peuvent transitoirement améliorer la symptomatologie, sans modification de la structure anatomique du canal.
Le canal d’Alcock apparaît ainsi non comme une cause unique et autonome de la névralgie pudendale, mais comme un révélateur fonctionnel de l’état de la dynamique tissulaire pelvienne. Il constitue un point de passage où les effets de la densification fasciale, de l’hypertonie musculaire et de la perte de glissement neural se combinent et deviennent cliniquement perceptibles (Stecco & Stecco, 2024).
Cette approche explique l’hétérogénéité des tableaux cliniques et l’errance diagnostique fréquente : un même canal anatomique peut être parfaitement toléré chez un sujet et devenir douloureux chez un autre, non en raison de sa morphologie, mais en fonction du régime mécanique global dans lequel il s’inscrit (Labat et al., 2008).
5. Chronicisation de la névralgie pudendale : verrouillage fonctionnel et dynamique auto-entretenue
La chronicisation de la névralgie pudendale ne peut être comprise à travers une lecture linéaire ou strictement lésionnelle. Dans de nombreux cas, la persistance de la douleur ne s’explique ni par une aggravation anatomique, ni par l’apparition d’une nouvelle atteinte structurelle, mais par l’installation progressive d’un régime mécanique défavorable au sein du système pelvien (Labat et al., 2008 ; Robert et al., 1998).
Ce régime se caractérise par une combinaison de contraintes posturales prolongées, en particulier la position assise, et par une réduction des micro-variations mécaniques nécessaires au maintien de la tolérance tissulaire. L’absence de variation suffisante transforme des contraintes initialement réversibles en contraintes dites figées, modifiant durablement la dynamique des tissus impliqués (Stecco & Stecco, 2024).
Sur le plan fonctionnel, cette situation entraîne l’activation de plusieurs boucles de rétroaction qui s’auto-entretiennent. La douleur neuropathique induit une hypertonie musculaire de protection, notamment au niveau des muscles profonds du bassin. Cette hypertonie augmente les contraintes mécaniques locales, réduit la mobilité relative des interfaces fasciales et aggrave la perte de glissement inter-tissulaire, exposant davantage le nerf pudendal à des micro-agressions répétées (Cholewa et al., 2024).
Parallèlement, la réduction des micro-mouvements et la persistance des contraintes favorisent une densification progressive des tissus. Cette réponse adaptative, initialement réversible, peut évoluer vers une rigidification fonctionnelle durable, parfois qualifiée de fibrose adaptative, qui limite encore la capacité des tissus à absorber et redistribuer les contraintes mécaniques (Stecco & Stecco, 2024).
Ces différents mécanismes ne constituent pas des phénomènes indépendants, mais s’inscrivent dans une organisation systémique. La perte de tolérance mécanique du nerf pudendal n’est pas la conséquence d’un événement unique, mais le résultat d’un déséquilibre durable entre contraintes posturales, adaptations tissulaires et capacités neuro-mécaniques. Ce déséquilibre abaisse progressivement le seuil de déclenchement de la douleur et explique la variabilité clinique observée, ainsi que la dépendance marquée à la posture et à la durée d’exposition (Labat et al., 2008).
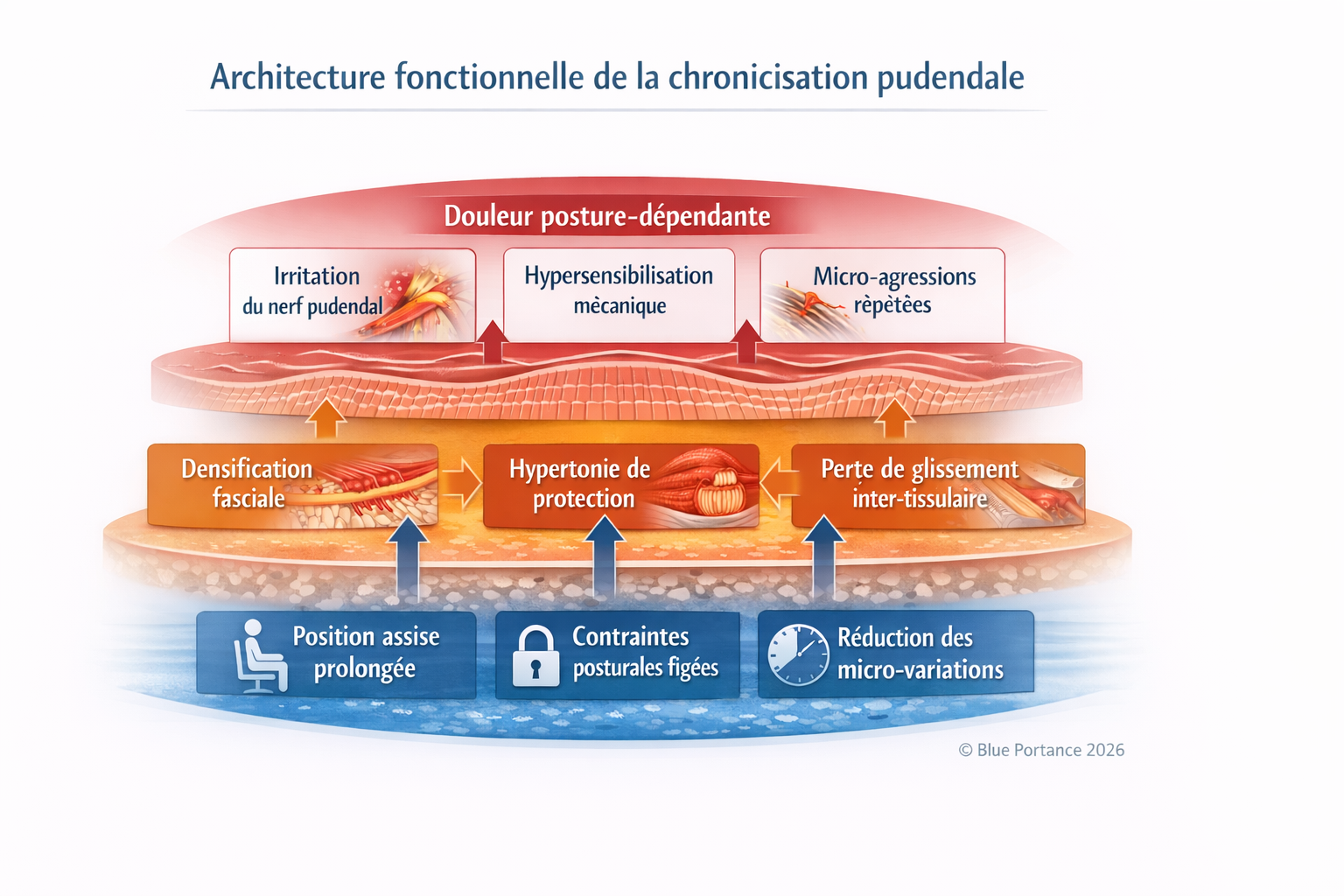
Ce modèle permet de comprendre pourquoi la névralgie pudendale échappe fréquemment aux approches purement structurelles et pourquoi l’imagerie peut rester normale malgré une symptomatologie sévère. Tant que le régime mécanique global demeure inchangé, les adaptations tissulaires et neuromusculaires continuent d’entretenir l’irritation nerveuse, indépendamment de toute intervention localisée (Stecco & Stecco, 2024).
La chronicisation apparaît ainsi non comme une fatalité inexpliquée, mais comme l’expression cohérente d’un système ayant perdu sa capacité d’adaptation mécanique. Cette lecture fonctionnelle constitue un préalable indispensable à toute stratégie visant à interrompre les boucles auto-entretenues de la douleur, en agissant non sur un point isolé, mais sur le régime mécanique dans son ensemble.
Références scientifiques
- Stecco A., Stecco C. (2024). Fascial densification and neuropathic pain: clinical implications.
- Butler D. (2000). The Sensitive Nervous System. Noigroup Publications.
- Cholewa J. et al. (2024). Myofascial entrapment in the Alcock’s canal.
- Robert R. et al. (1998). Anatomical basis of pudendal nerve entrapment.
- Blue Portance — Modèle SBNFA™ (2026). NEURO-ANATOMIE — Partie V.


