1. Origines radiculaires et rôle neuro-fonctionnel
Le nerf pudendal naît des branches antérieures des racines sacrées S2, S3 et S4. Cette origine pluriradiculaire est déterminante : elle associe des fibres somatiques (sensitives et motrices) et des fibres du système nerveux autonome, notamment parasympathiques (Robert et al., 1998).
Cette double composante explique pourquoi la névralgie pudendale ne se limite pas à une douleur localisée. Une irritation du nerf peut s’exprimer par des brûlures, des décharges électriques, mais aussi par des troubles fonctionnels urinaires, anorectaux ou sexuels, sans lésion visible de l’organe concerné (Labat et al., 2008/2023).
Les racines S2–S4 participent aux fonctions de stockage et d’évacuation (vessie, rectum) ainsi qu’à la sensibilité périnéale. Toute contrainte mécanique exercée sur le nerf pudendal peut donc produire un retentissement sensoriel et fonctionnel disproportionné (Labat et al., 2008/2023).
2. Un trajet sinueux à haute vulnérabilité mécanique
Le nerf pudendal possède un trajet singulier : il quitte la cavité pelvienne pour y revenir presque immédiatement. Ce détour anatomique, indispensable à son rôle fonctionnel, constitue également une vulnérabilité biomécanique (Robert et al., 1998).
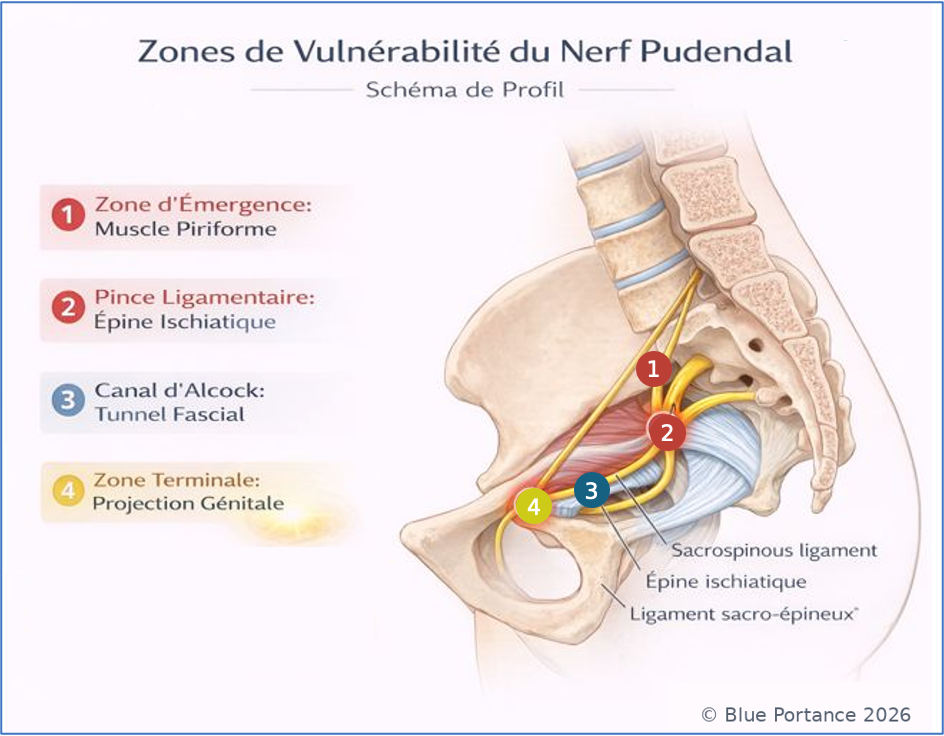
Après son émergence, le nerf sort du bassin par la grande échancrure sciatique, contourne l’épine ischiatique, puis réintègre le pelvis par la petite échancrure sciatique pour cheminer dans le canal d’Alcock (Robert et al., 1998).
Ce parcours impose au nerf de franchir plusieurs zones étroites, sensibles aux variations posturales, aux tensions musculaires et à la géométrie pelvienne. À chaque changement de position, notamment en station assise prolongée, le nerf peut être soumis à des forces de cisaillement et de compression variables (Labat et al., 2008/2023).
3. Les branches terminales et la logique de projection
À l’issue de son trajet principal, le nerf pudendal se divise en trois branches terminales, souvent décrites comme le trident pudendal (Labat et al., 2008/2023).
- Nerf rectal inférieur : innerve le canal anal et peut expliquer des douleurs anorectales, sensations de corps étranger ou brûlures profondes.
- Nerf périnéal : innerve notamment l’urètre et le périnée ; il peut être associé à des brûlures urinaires/périnéales sans infection objectivable (Labat et al., 2008/2023).
- Nerf dorsal du clitoris ou du pénis : assure la sensibilité fine génitale ; il peut être associé à des décharges électriques, hypersensibilités ou douleurs au contact.
Cette organisation explique pourquoi la douleur est souvent ressentie « à distance » du conflit réel : le cerveau interprète le message nociceptif au niveau de la zone terminale, alors que la contrainte mécanique peut se situer plus haut sur le trajet (Labat et al., 2008/2023).
4. Le nerf dans son environnement fascial
Le nerf pudendal ne “flotte” pas dans le bassin : il est intimement lié aux fascias pelviens, notamment au fascia de l’obturateur interne qui participe à la constitution du canal d’Alcock (Cholewa et al., 2024).
Les fascias permettent un glissement neural physiologique. Lorsque la matrice fasciale se densifie, la mobilité tissulaire diminue : le nerf peut être mécaniquement agressé à chaque micro-mouvement, sans qu’il n’existe nécessairement une lésion anatomique visible (Stecco & Stecco, 2024).
Une imagerie normale n’exclut pas une souffrance du nerf : une partie du problème peut relever d’une dysfonction de glissement et d’un environnement tissulaire altéré (Stecco & Stecco, 2024).
5. Réserve adaptative et seuil de décompensation
Le nerf pudendal possède une certaine capacité d’adaptation : il peut tolérer des contraintes ponctuelles sans douleur. La névralgie apparaît lorsque la somme des agressions (posture, contraintes mécaniques, tensions musculaires, densification fasciale) dépasse une réserve adaptative individuelle (Labat et al., 2008/2023).
Cette notion est essentielle pour comprendre pourquoi certaines personnes développent une névralgie sans traumatisme identifiable, et pourquoi la douleur peut s’installer progressivement au fil du temps.
- Labat, J.-J., Riant, T., Robert, R., et al. (2008; mise à jour 2023). Diagnostic criteria for pudendal neuralgia by pudendal nerve entrapment (Nantes criteria). Références cliniques et critères diagnostiques de la NP.
- Robert, R., Prat-Pradal, D., Labat, J.-J., et al. (1998). Anatomical basis of pudendal nerve entrapment. Surgical and Radiologic Anatomy. Bases anatomiques du trajet, zones de vulnérabilité et conflits possibles.
- Cholewa, J., et al. (2024). Myofascial entrapment in the Alcock’s canal: The role of pelvic floor hypertonia. Éléments sur l’environnement myofascial et le canal d’Alcock.
- Stecco, A., & Stecco, C. (2024). Fascial densification and neuropathic pain: clinical implications. Modèle de densification et lien avec la perte de glissement.


